化學元素週期表會有完成的一天嗎?

圖像來源,AFP via Getty Images
- Author, 蘇菲・阿布杜拉(Sophie Abdulla)
- Role, BBC國際部
- 閱讀時間: 3 分鐘
上一次元素週期表新增成員是在十年前,當時第113、115、117和118號元素被正式納入。
國際監管機構還做出了一件此前只做過一次的事情:將其中一個元素以仍在世的物理學家命名。
尤里·奧加涅相(Yuri Oganessian)領導的俄美研究團隊於2002年發現第118號元素(奧加涅松,oganesson)。由於該元素極度具放射性,只製造出很少它的原子,因此花了多年時間才確認其存在。
人們不禁會問:為何過去10年沒有新的元素加入?會不會有一天,元素週期表被確認完成?
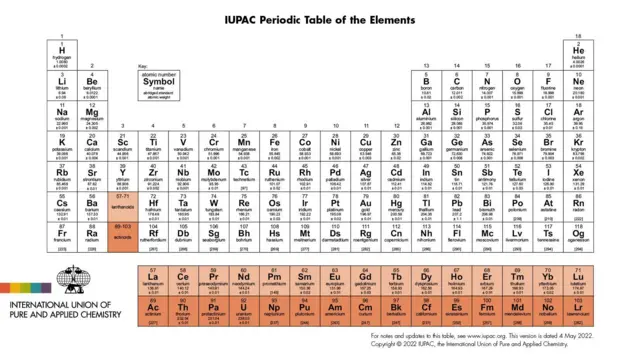
圖像來源,International Union of Pure and Applied Chemistry (IUPAC)
什麼是元素週期表?
元素週期表本質上是一張化學元素的地圖,由一格格標有縮寫化學符號的方框組成,並且隨時間推移不斷被修訂。
元素是一種由單一類型原子構成的純物質。原子是構成物質的基本單位,其結構包括一個原子核——通常含有帶正電的質子和不帶電的中子——以及周圍帶負電的電子。
週期表中的各種元素構成了宇宙中我們所知的一切——包括人類本身。
19世紀初,人類已發現許多元素,但尚未有系統的整理方式。許多學者試圖改變這一情況。
其中之一是英國化學家約翰·紐蘭茲(John Newlands)。
他按照原子重量排列元素,發現每隔八個元素就會出現性質相似的情況。例如鋰、鈉和鉀彼此間隔八位,且對水的反應相似。
他稱此為「八度定律」。

圖像來源,Oxford Science Archive/Print Collector via Getty Images
被廣泛視為「元素週期表之父」的俄國化學家德米特里·門捷列夫(Dmitri Mendeleev)進一步整理這一概念,提出了「週期律」。
他在1869年建立了一個以原子重量排列的框架。
與紐蘭茲不同的是,門捷列夫為尚未發現的元素預留空位。後來這些元素被發現,證明了他的理論。
如今,元素是依據其原子序——即原子核中的質子數——來定義與排列。氫有1個質子,而奧加涅松則有118個。
同一欄的元素具有相似的化學性質,例如它們和其他物質的反應方式也相似。它們的物理性質(例如熔點)也常呈現出規律,使科學家能預測其行為。例如工程師就可以依此選擇橋樑或飛機的材料。

圖像來源,Jiojio via Getty Images
若科學家認為發現了新元素,需經由國際純粹與應用化學聯合會(IUPAC)確認其存在並納入週期表,這一過程可能需要數年時間。
目前普遍認為,地球上所有天然存在的元素都已被發現,它們構成了週期表的大部分。更重的元素則必須在實驗室中,透過組合兩種較輕元素人工製造。
隨著科技進步,科學家能製造出更多超重元素。理論上雖然仍可嘗試創造新元素,實際難度卻越來越高。
製造新元素
倫敦國王學院成像化學與生物學系主任菲爾·布洛爾教授(Prof Phil Blower)教授表示,為了將較輕元素結合成更重的新元素,「我們必須使用能量更高的環境,這意味著建造更大型的回旋加速器或加速器」。
他指出:「元素變得越大越重,就越加不穩定,因為原子核中的質子彼此排斥。」

圖像來源,San Francisco Chronicle/Hearst Newspapers via Getty Images
原子核中質子與中子的比例,決定其穩定性。帶正電的質子彼此排斥,但中子的存在可以幫助它們維持結合。
倫敦國王學院研究員辛齊婭·伊姆貝蒂(Cinzia Imberti)解釋:「當你製造愈重的元素時,就是在增加更多質子,因此需要更多中子來防止原子核崩解。」
元素可以擁有不同數量的中子,這些變體稱為同位素。不穩定的同位素具有放射性,會透過釋放輻射而衰變。
圖像來源,KTSDESIGN/Science Photo Library via Getty Images
卡迪夫大學化學家喬納森·洛克(Jonathan Rourke)指出:「所有比鉛(元素82)更重的元素都是放射性的,本質上不穩定,會分解。」
「我們就算能製造出其中一個原子,它也無法維持太久。」他說。
伊姆貝蒂表示,尤其是從第100號元素(鐨)開始更是如此:「你只能製造出少量原子,了解一些基本性質,但它們沒有實際用途。」
儘管如此,科學界仍持續尋找新的元素——未來可能開啟週期表的新一行。
目前對119號與120號元素的多次嘗試均未成功,但各研究團隊仍在努力。科學家認為,探索這些極端元素有助於加深對原子運作、核穩定極限的理解,並檢驗核物理理論。
「你不僅要問我們能否將它製造出來,」伊姆貝蒂說,「還要考慮它是否能存在足夠長時間,讓我們能真正觀察並了解它,在消失之前……獲得一點有用的資訊。」














